机体衰老是由身体的大多数细胞、组织或器官的逐渐老化引起的,免疫系统也不例外。免疫系统的失调和恶化,即所谓的“免疫衰老”,使老年人对新病原体感染、自身免疫以及慢性非免疫性疾病(包括心血管和神经退行性疾病、癌症和2型糖尿病)抵抗力减弱。
T细胞和B细胞衰老表型
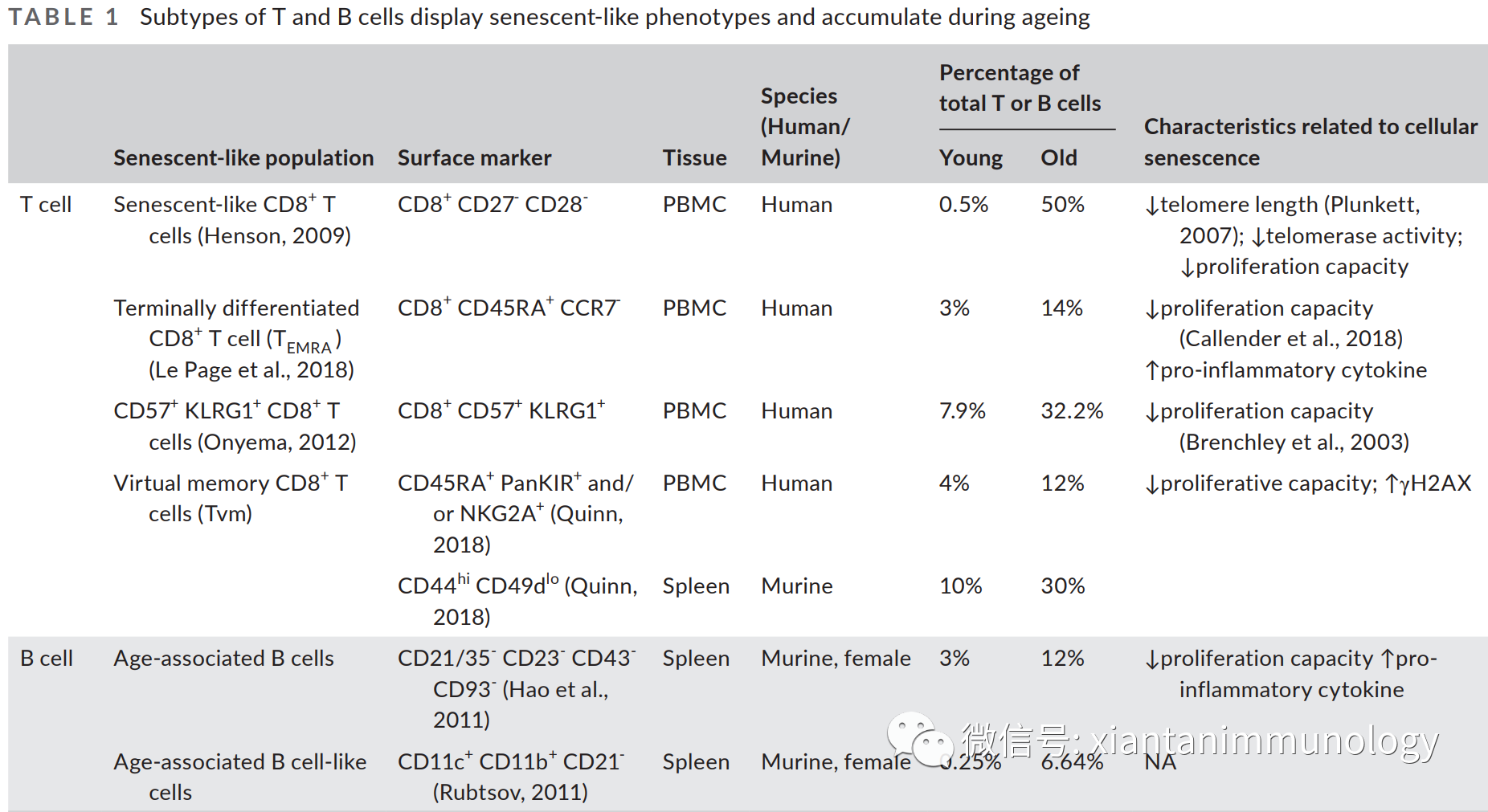
免疫细胞衰老机制
随着步入老年,人体对感染、恶性肿瘤和疫苗接种的免疫反应受损,并伴随着慢性低度炎症,一起称为免疫衰老。免疫衰老的分子和细胞机制,大多是未知的。
应激源诱导的下游信号,最终汇聚到p53/p21CIP和/或p16INK4a/pRB通路,直接作用于周期蛋白依赖的激酶,来抑制细胞周期。
DNA损伤以p53依赖的方式上调p21CIP水平,而p38-MAPK介导的线粒体ROS水平的增加刺激p16INK4a的表达。
2. 端粒损耗
端粒是线性染色体末端的特殊结构,在哺乳动物细胞中,它由典型的端粒DNA重复序列(TTAGGG)和相关蛋白组成。
在DNA复制过程中,复制机制不能完全复制端粒DNA,导致每次端粒缩短,称为“末端复制问题”。
一旦端粒DNA缩短到一个阈值以下,它可能会导致DNA断裂和复制性衰老。因此,端粒缩短是导致端粒功能障碍的一个原因。
 在免疫系统中,淋巴细胞和粒细胞的平均端粒长度均随着衰老而减少,淋巴细胞的端粒缩短更明显。
同亚型的人CD8+T淋巴细胞的端粒长度也有所不同。初始细胞通常比高分化细胞端粒更长,从而导致更高的增殖潜力。
端粒酶是一种维持端粒长度的逆转录酶。因为高端粒酶活性,所以永生细胞系、生殖细胞、干细胞或胎儿发育早期的细胞,可逃避端粒功能障碍引起的复制衰老。
而在静息淋巴细胞中,端粒酶活性通常较低,但丝裂原刺激可以瞬时上调端粒酶活性。一项研究表明,随着年龄的增长,静止的T细胞和B细胞的端粒酶活性下降。
在免疫系统中,淋巴细胞和粒细胞的平均端粒长度均随着衰老而减少,淋巴细胞的端粒缩短更明显。
同亚型的人CD8+T淋巴细胞的端粒长度也有所不同。初始细胞通常比高分化细胞端粒更长,从而导致更高的增殖潜力。
端粒酶是一种维持端粒长度的逆转录酶。因为高端粒酶活性,所以永生细胞系、生殖细胞、干细胞或胎儿发育早期的细胞,可逃避端粒功能障碍引起的复制衰老。
而在静息淋巴细胞中,端粒酶活性通常较低,但丝裂原刺激可以瞬时上调端粒酶活性。一项研究表明,随着年龄的增长,静止的T细胞和B细胞的端粒酶活性下降。
3. 衰老分泌表型因子
衰老相关的分泌表型(Senescence-associated secretory phenotype,SASP)是衰老细胞的另一个典型特征。衰老细胞分泌一系列可溶性因子,包括促炎细胞因子、趋化因子、生长因子和蛋白酶。
在年轻人中,SASP通过促进肌成纤维细胞分化和伤口愈合来促进组织稳态。然而,衰老细胞随着年龄的增长而积累,慢性SASP促进邻近细胞的退行性变化和衰老相关病理。
SASP因子可能产生促炎环境并招募免疫细胞,免疫细胞可能进一步产生更多的促炎细胞因子,并加重与衰老相关的病理。
人类终末分化的TEMRA细胞和小鼠的TEMRA-like虚拟记忆CD8+T细胞,在衰老晚期,表现出独特的高炎症分泌特征,SASP是由p38-MAPK信号通路调控的。

大部分SASP因子可能起源于先天免疫系统。从小鼠骨髓中分离出的老化的CD14+髓系细胞显示36个SASP相关mRNA的表达增加。同样,老年中性粒细胞中促炎(IL1α、IL-1β、IL-6、TNFα和IFNγ)的合成显著增加。
4. 半乳糖苷酶
衰老相关半乳糖苷酶(SA-β-gal)活性和p16INK4a的表达,作为检测细胞衰老的生物标志物,正常情况下,溶酶体-半乳糖苷酶在pH4.0~4.5之间显示出-半乳糖苷的水解活性峰值。在衰老细胞中,由于酶的积累,这种活性在pH值为6.0时可检测到。
5. 脂褐质
脂褐素是一种富集在老年神经元、肌肉和皮肤的自身荧光脂肪色素。
虽然脂褐素的性质和结构表现出组织特异性和时间异质性,但它普遍由脂质、金属和错误折叠蛋白组成。
随着时间的推移,脂质色素在溶酶体和细胞质中积累,这一方面,是一种特定的细胞衰老模式,另一方面,加重了衰老过程中溶酶体降解途径的缺陷。
老年小鼠腹腔巨噬细胞、小胶质细胞和T细胞中的脂褐素水平均显著高于年轻小鼠。
活性氧(ROS)是指一类自由基和非自由基氧。大多数细胞ROS(cROS)是通过线粒体有氧呼吸内源性产生的。其他环境刺激,如生长因子、炎症细胞因子和电离辐射,也可以诱导cROS。
过量的ROS会对各种大分子造成氧化损伤,包括DNA、蛋白质和脂质。细胞通过多种抗氧化系统严格调节cROS水平,并维持氧化还原稳态。然而,在衰老过程中,细胞的氧化剂/抗氧化比值变得不平衡,通常有利于氧化剂和过量的ROS累积,从而损害细胞的稳态和功能。
电子传递链中,线粒体ATP是cROS的主要生产者,线粒体DNA(mtDNA)和蛋白质特别容易受到ROS的影响。
T细胞的激活和分化涉及代谢重编程。在人类初始记忆和中枢记忆CD8+T细胞中,mROS水平与衰老显著相关,来自老年供体的抗体分泌细胞显示出mROS的增加。
7. DNA损伤
细胞不断暴露于DNA损伤剂中,包括化学诱变剂、辐照和氧化应激。为了保持基因组的稳定性,一种被称为DNA损伤反应(DDR)的进化保守途径可以感知DNA损伤,并招募修复机制来修复DNA损伤。
如果DNA损伤持续存在,细胞可能会发生凋亡或进入细胞衰老。可以推断,一些衰老细胞可能比非衰老细胞含有更多的DNA损伤和更高的DDR水平。
8-氧鸟嘌呤(8-oxoG)是由鸟嘌呤被ROS修饰引起的最常见的DNA损伤之一。
DNA损伤也会导致表观遗传学的变化。H2AX是组蛋白H2A变异,检测H2AX病灶可以反映DNA双链断裂、基因组不稳定性和端粒功能障碍。
8. 蛋白质稳态
内质网具有未折叠蛋白反应(UPR),这是一种重要的应激触发途径,可以抑制蛋白质聚集,并促进细胞稳态。
三个重要的感受器:IRE1α(inositol-requiring enzyme 1α),PERK(PKR-like ER-resident kinase),ATF6α(activating transcription factor 6α)。
它们的激活与结合免疫球蛋白蛋白(BiP,GRP-78)的分离有关,增加分子伴侣活性、翻译抑制、改善蛋白质稳态。蛋白质稳态依赖于UPR下游的降解和再循环机制的激活,如泛素蛋白酶体系统和自噬,这决定了细胞的死亡或存活。
衰老伴随着UPR的失调,这导致了蛋白质稳态的丧失。检测到低BiP水平(包括mRNA或蛋白质)是分子识别免疫细胞衰老的指标。较低水平的BiP也会引起UPR激活,最终导致蛋白质翻译受损。
泛素-蛋白酶体系统(UPS)是细胞内蛋白分解代谢途径的主要组成部分。通过去除错误折叠或损伤的蛋白质,它有助于在各种形式的细胞应激下维持蛋白质稳态。
UPS介导的降解包括两个阶段:泛素化和蛋白酶体介导的降解。泛素标记蛋白质底物,将其传递到蛋白酶体进行降解。蛋白酶体包含20S“核心”催化室和19S“帽”调节颗粒,它们结合多泛素化底物并将其转移到中央腔室中。
在免疫细胞中,一种特殊形式的蛋白酶体,被称为免疫蛋白酶体,在消化病毒来源的细胞内蛋白中起着至关重要的作用,它有助于产生小肽,进一步MHC-I介导的抗原递呈。
衰老的人类淋巴细胞显示蛋白酶体功能下降,主要是由于蛋白酶体亚基的翻译后修饰(糖基化、脂质过氧化产物偶联和泛素化)。此外,TCR刺激的衰老CD4+T细胞也不能诱导蛋白酶体亚基基因的转录上调。在来自老年供体的T细胞中,蛋白酶体活性降低导致TNFα刺激下IκBa降解受损,导致NF-κB信号通路增加和IL2R上调。
总结:细胞衰老标志物及检测方法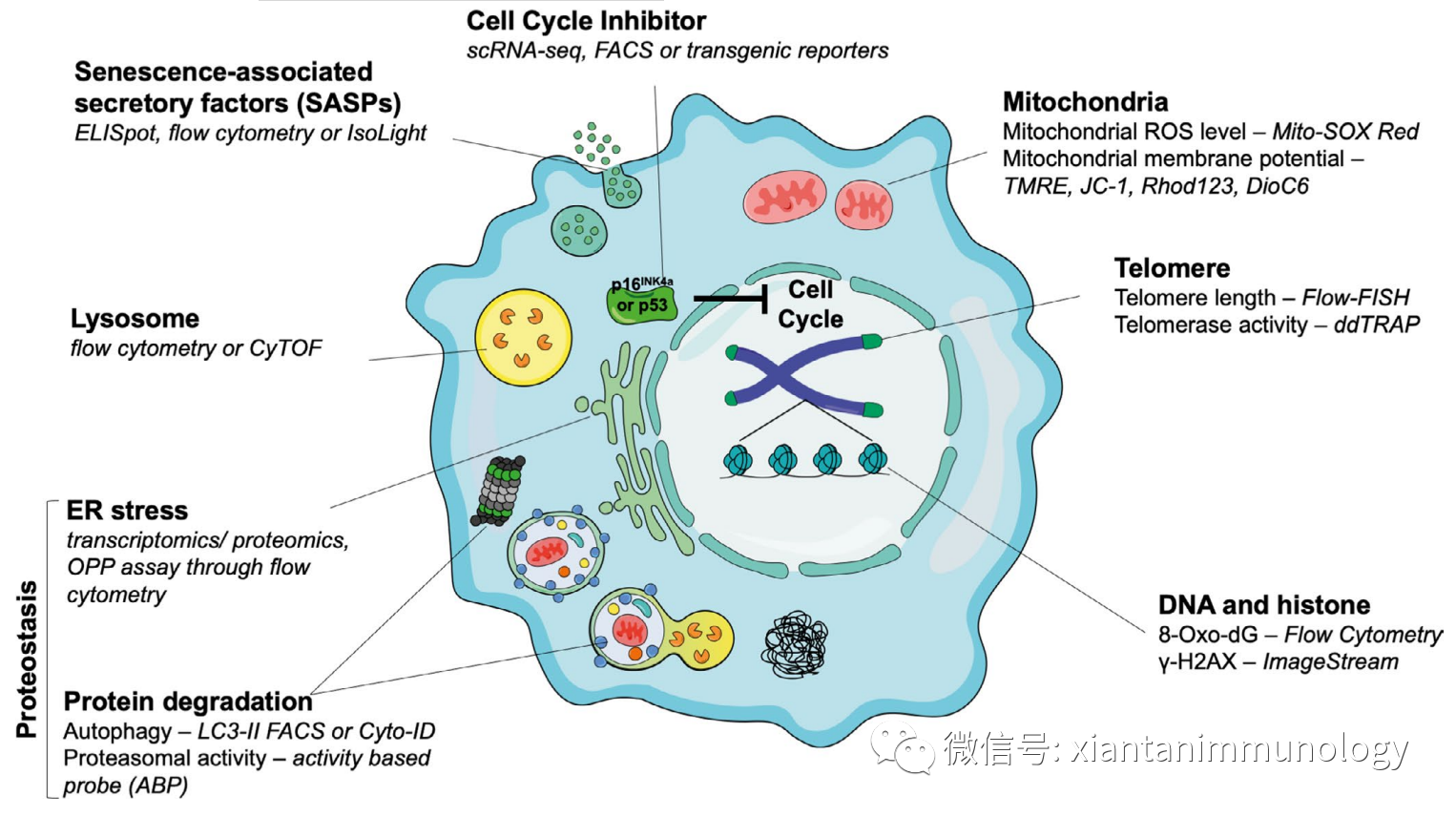
主要参考文献
-
Shay, J. W., & Wright, W. E. (2019). Telomeres and telomerase: Three decades of progress. Nature Reviews Genetics, 20, 299–309. https:// doi.org/10.1038/s41576-019-0099-1
-
Marcia Bellon and Christophe Nicot ,Telomere Dynamics in Immune Senescence and Exhaustion Triggered by Chronic Viral Infection,Viruses 2017, 9, 289
-
Kumari R and Jat P (2021) Mechanisms of Cellular Senescence: Cell Cycle Arrest and Senescence Associated Secretory Phenotype. Front. Cell Dev. Biol. 9:645593. doi: 10.3389/fcell.2021.645593
-
Dingxi Zhou et al,Hallmarks and detection techniques of cellular senescence and cellular ageing in immune cells,Aging Cell. 2021;20:e13316